苯肼类化合物的光诱导缩环
苯环的骨架修饰是利用芳香性化合物的重要手段之一。但是,苯环自身热力学稳定性高,导致其发生骨架缩环重排极具挑战性。近日,兰州大学胡安华和郭婧婧团队提出了一种光热串联活化策略,利用阻断的Fischer吲哚合成法中原位生成的吸光中间体易被光照激发的性质,实现了苯肼类化合物的光诱导缩环,改变了经典的Fischer吲哚合成反应路径,为多取代吡啶的模块化合成提供了一种新方法,为反应中间体参与的光促反应设计提供了一种新思路。2026年1月30日,相关成果以“Photoinduced benzene ring contraction of arylhydrazines for the synthesis of fused pyridines”为题,发表在Nature Synthesis期刊上。论文通讯作者是胡安华和郭婧婧,第一作者是李坤。
目前,苯环的缩环反应大多存在着反应条件苛刻和高张力反应中间体难以有效转化等亟待攻克的研究难点。研究团队将研究目标锁定在芳基肼类化合物的活化,提出了一种光热串联活化模式,利用反应中间体的吸光特性来设计光促缩环反应(图1)。该接力的活化模式不需要额外使用光敏剂,通过光开关设计就能实现在反应中原位控制反应中间体的反应路径。经典的Fischer吲哚合成法被广泛应用在有机合成中,其中的[3.3]-重排过程为苯肼中苯环的去芳构化提供了有效手段。通过光照激发反应中原位产生的吸光中间体,使苯环的骨架重排成为主要的反应路径,反应活性从而得以被精准调控。该反应底物适用性广,环酮、开链的酮以及醛都能作为有效的C2供体,为氮杂茚环的模块化合成提供了十分便利的方法。
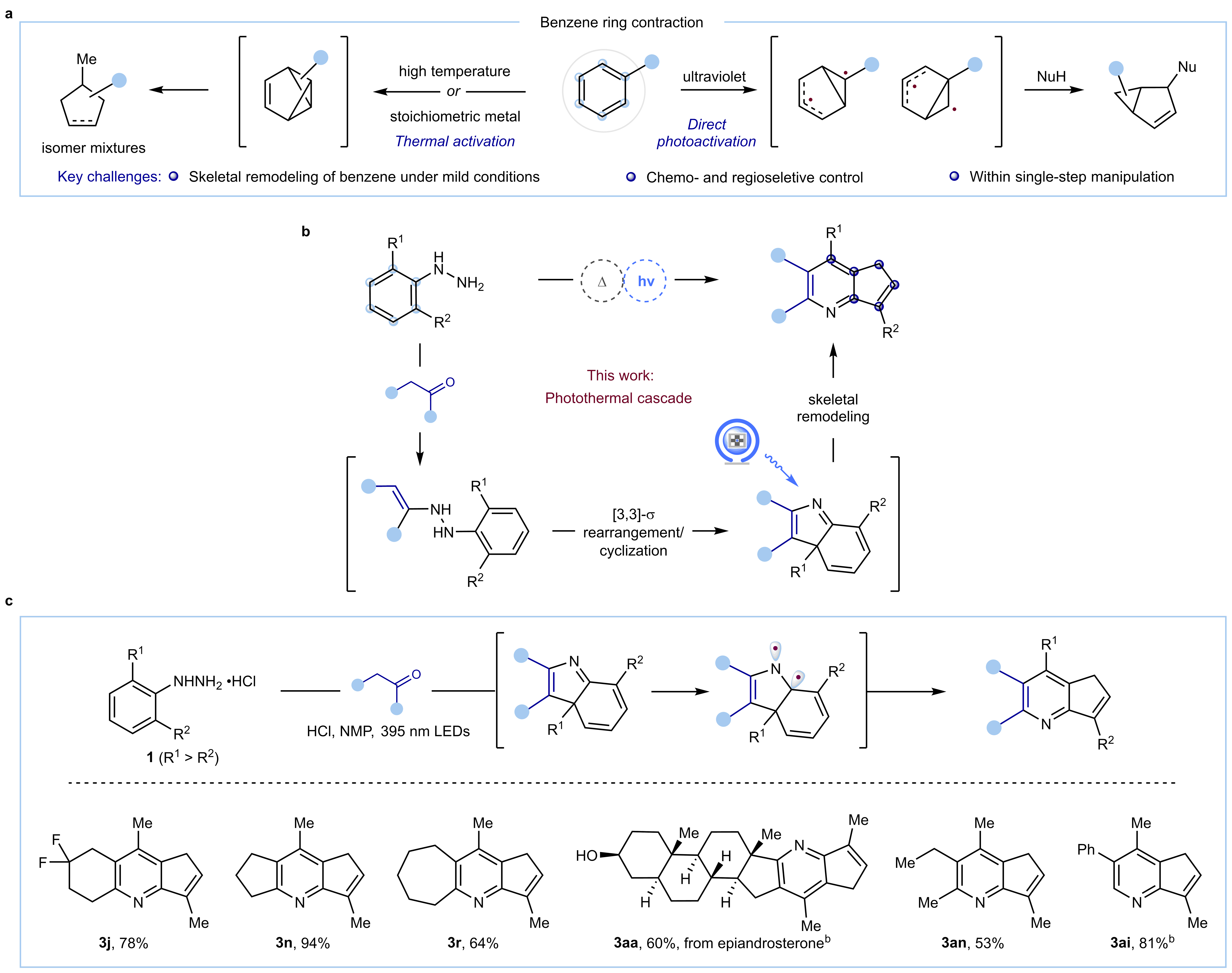
图1:苯环的缩环重排反应设计。
该反应能在实验室以克级规模放大,所得到的氮杂茚环产物可以经过一步,高效转化为其他多种药物分子骨架,比如8-羟基喹啉和1,7-萘啶等。研究人员还将该反应应用到一些药物分子、其类似物以及手性配体材料的合成中,展现了该反应优秀的实用性,比如利用乙醛为C2供体,应用该方法由萘肼出发,经过两步反应就能实现药物分子onychine的合成等。此外,研究人员对反应的机理进行了细致的研究,他们通过光谱实验、反应动力学实验和同位素标记实验等对反应中间体的反应行为进行了刻画,通过理论计算进一步验证了苯环缩环反应的历程(图2)。
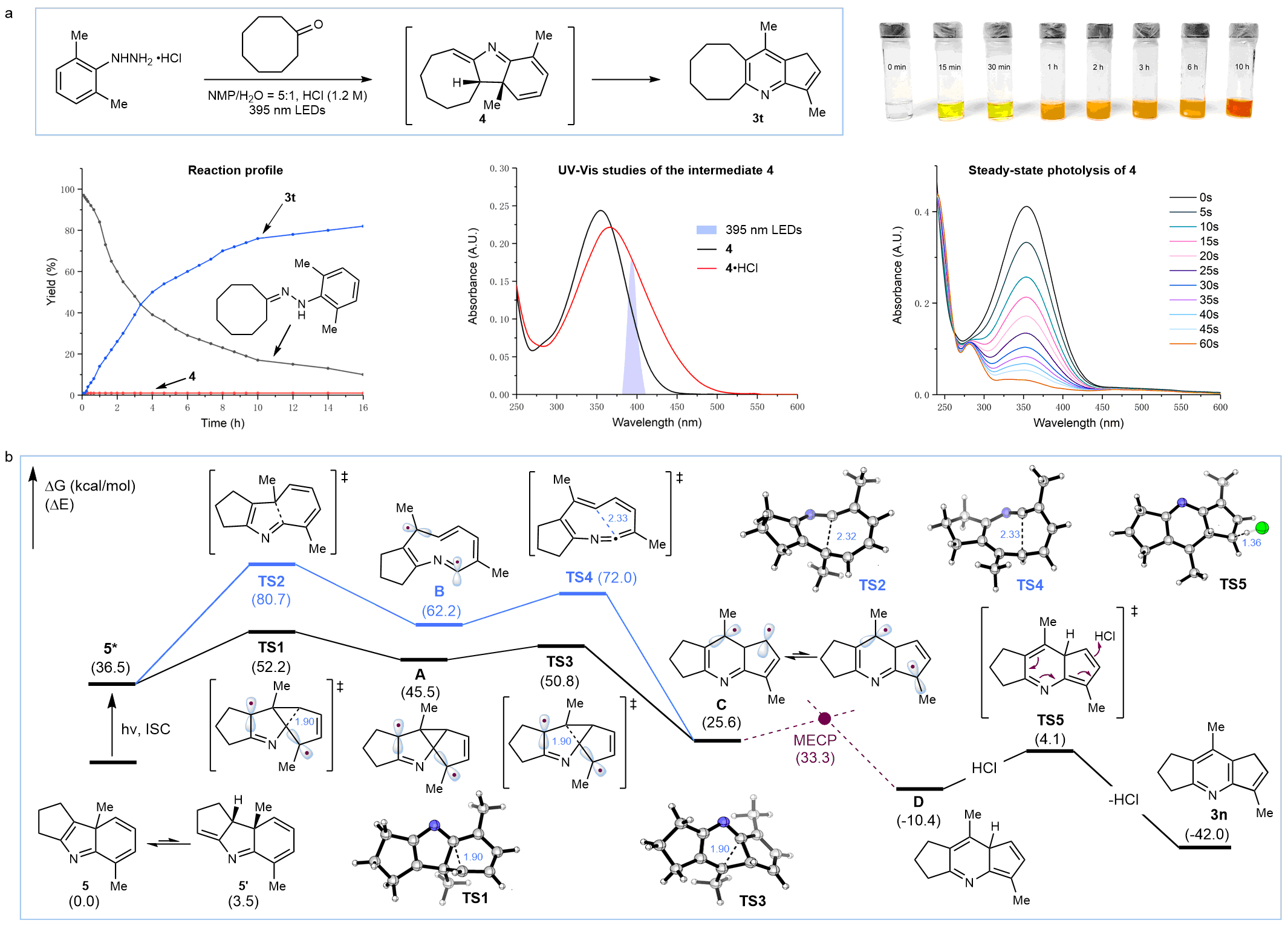
图2:苯环缩环反应机理研究。
总体而言,该项研究中作者以苯肼类化合物的缩环反应为切入点,在经典的Fischer吲哚合成法基础上,通过对反应中可能的中间体仔细分析,提出了光热串联活化策略,实现了反应路径的精准调控,为多取代吡啶化合物的合成提供了新方法。该反应条件温和,展示了化学工作者对痕量的反应中间体活性调控能够策略性地改变反应路径的新思路,在药物分子合成和材料科学领域具有广阔的应用前景。(来源:科学网)
相关论文信息:https://doi.org/10.1038/s44160-025-00976-4
